«Флуометрия
в анализе объектов окружающей среды»ОГЛАВЛЕНИЕ
ВВЕДЕНИЕ
ГЛАВА 1. ТЕОРЕТИЧЕСКИЕ
ОСНОВЫ ФЛУОМЕТРИИ (ЛЮМИНЕСЦЕНЦИИ)ГЛАВА 2. ОБЛАСТИ
ПРИМЕНЕНИЯ ФЛУОМЕТРИИ В АНАЛИЗЕ ОБЪЕКТОВ ОКРУЖАЮЩЕЙ СРЕДЫГЛАВА 3. СОВРЕМЕННОЕ
ОБОРУДОВАНИЕЛИТЕРАТУРА
ВВЕДЕНИЕ
Люминесцентный анализ обладает рядом особенностей, которые
отличают его от всех других видов анализа. Люминесцентный анализ необычайно
чувствителен. С его помощью можно обнаружить в пробе присутствие вещества с
концентрацией ~10 — 10 – 10 — 11 г/г. Это более чем на три
порядка превосходит чувствительность эмиссионного спектрального анализа, что
позволяет работать с исчезающе малыми количествами исследуемого вещества ~10 — 12
– 10 — 15 г. С помощью люминесцентного анализа можно исследовать очень
небольшие объемы раствора, а также анализировать мельчайшие крупинки порошков,
в которых содержатся следы других люминесцирующих веществ.Важным преимуществом люминесцентного анализа являются его простота
и скорость, во много раз превосходящие скорость химического анализа.ГЛАВА 1. ТЕОРЕТИЧЕСКИЕ ОСНОВЫ ФЛУОМЕТРИИ (ЛЮМИНЕСЦЕНЦИИ)
Флуометрия (люминесценция) является одним из широко
распространенных в природе видов излучения. Помимо люминесценции известны и
другие свечения, которые, однако, существенно отличаются от нее, например, температурное
излучение, свечения, наблюдаемые при быстром движении электрических зарядов
(тормозное излучение, Свечение Вавилова — Черенкова) и т. п.Люминесценцией называют избыток излучения над температурным при
условии, что избыточное излучение обладает конечной длительностью, превышающей
период световых колебаний (~ 10 — 10 сек).Это определение основано на противопоставлении люминесценции
температурному излучению, свойства которого хорошо известны. Вместе с тем оно
указывает на наличие у люминесценции конечной длительности послесвечения,
превышающей период световых колебаний. Это условие позволяет отличать
люминесценцию от отражения, рассеяния и излучения Вавилова-Черенкова, которые
являются практически безынерционными.Очень многие вещества обладают способностью люминесцировать. При
этом они могут находиться в газообразном, жидком и твердом состояниях.
Простейшими из них являются газы и пары различных элементов (О2, I2, Na2 и т. д.).
Люминесцентными свойствами обладают соли некоторых веществ (редкоземельных
элементов, ураниловых соединений), ароматические соединения (нафталин, бензол,
антрацен, и производные и др.), растворы ряда красителей, а также многие другие
вещества. Особый класс люминесцирующих соединений составляют так называемые
кристаллофосфоры — неорганические вещества (например. ZnS, CaS и др.), в
кристаллическую решетку которых введены ионы тяжелых металлов (например, Ag, Cu, Mn и др.).Для того чтобы вещество начало люминесцировать, к нему необходимо
извне подвести определенное количество энергии. Тогда его частицы переходят в
новое, более богатое энергией, возбужденное состояние, в котором они пребывают определенное
время, после чего вновь возвращаются в невозбужденное состояние, отдавая при этом
часть энергии возбуждения в виде квантов люминесценции.Энергия возбуждения может быть подведена к веществу различными
способами. В зависимости от метода возбуждения возникающее свечение получает
различные названия. Так, при возбуждении свечения оптическими частотами оно
носит название фотолюминесценции; свечение, возникающее под действием катодных
лучей, называется катодолюминесценцией; при возбуждении веществ рентгеновыми
лучами возникает рентгенолюминесценция; при облучении их лучами радиоактивных
элементов наблюдается радиолюминесценция; свечение, появляющееся при химических
реакциях, получило название хемилюминесценции; свечение, возникающее под
действием электрического поля, называется электролюминесценцией. Люминесценция
может быть получена и с помощью других источников возбуждения.Распределение молекул по колебательным уровням как
невозбужденного, так и возбужденного электронного состояния описывается
формулой Больцмана:
(1)
где N0 — полное число всех молекул; Ni — число молекул на
уровне i;
Еi — значение колебательной энергии, соответствующее уровню i. Если при некоторой
температуре Ei >> kT, то в соответствии с формулой (1) подавляющая
часть молекул должна находиться на нулевом колебательном уровне. Для комнатной
температуры это условие обычно выполняется, что позволяет считать, что в этом случае
практически все молекулы находятся на нулевом уровне. Таким образом, по мере
роста номера уровня число находящихся на нем молекул быстро убывает.Оптические свойства люминесцирующих веществ описываются с помощью
целого ряда характеристик. Сюда относятся спектры поглощения и люминесценции,
поляризация свечения (и поляризационные спектры), выход люминесценции,
длительность возбужденного состояния молекул, закон затухания свечения и кривые
термического высвечивания.1.1 Спектры поглощения
Спектром поглощения вещества называется совокупность коэффициентов
поглощения, характеризующих его поглощательную способность к лучам оптического
диапазона частот. Коэффициенты поглощения определяются из закона Ламберта—Бера.Спектры поглощения люминесцирующих веществ крайне разнообразны.
Одни из них имеют вид очень узких полос (растворы солей редкоземельных
элементов), другие — более широких полос с четко выраженной колебательной
структурой (растворы ураниловых солей), наконец, спектры поглощения многих
веществ представляют собой широкие размытые полосы, структуру которых не
удается выяснить даже при низких температурах (растворы красителей).Спектры поглощения могут существенно меняться при изменении
концентрации раствора, его кислотности или щелочности (величины его рН), природы
растворителя, температуры и ряда других факторов.Спектры люминесценции.
Спектром люминесценции называется распределение излучаемой
веществом энергии по частотам или длинам волн. Подобно спектрам поглощения,
интенсивность и форма спектров люминесценции у разных веществ могут быть весьма
различными, и они могут существенно изменяться при вариации тех же параметров
(концентрации, величины pH раствора и т. д.)1.2 Выход люминесценции
Выход люминесценции характеризует эффективность трансформации
возбуждающего света в свет люминесценции в исследуемом веществе. Различают энергетический
и квантовый выходы люминесценции. Энергетическим выходом люминесценции называют
отношение излучаемой веществом энергии Eл к поглощенной энергии
возбуждения Еп:
(2)
Квантовым выходом люминесценции называют отношение числа квантов
люминесценции, излученных веществом Nл к числу поглощенных квантов возбуждающего света Nп:
(3)
Выход люминесценции очень чувствителен к внешним воздействиям,
которые во многих случаях приводят к тушению свечения. Так, известно тушение
люминесценции посторонними примесями, возникающее при добавлении к раствору
посторонних веществ — тушителей. Тушителями могут служить KI, анилин и другие
вещества. В результате взаимодействия возбужденных молекул люминесцентного
вещества с молекулами тушителя возникает безизлучательный размен энергии
возбуждения. Безизлучательные переходы развиваются и при увеличении температуры
раствора, обуславливая появление температурного тушения.В большинстве случаев увеличение концентрации также приводит к
тушению свечения. При этом концентрационное тушение обычно начинает проявляться
лишь при достижении некоторой пороговой концентрации, величина которой
характерна для исследуемого вещества. В более разведенных растворах выход
люминесценции не зависит от концентрации. Это обстоятельство может быть
использовано в люминесцентном анализе при подборе оптимальных условий его
проведения.Концентрационное тушение имеет двоякую природу. С одной стороны,
при увеличении концентрации могут образовываться ассоциированные молекулы, не
обладающие люминесцентной способностью, но поглощающие энергию возбуждения. С
другой стороны, между возбужденными и невозбужденными молекулами может
осуществляться индукционный перенос, или, как говорят, миграция энергии
возбуждения. Такой перенос энергии возбуждения прежде всего на нелюминесцентные
ассоциаты приводит к развитию концентрационного тушения.Известны и другие виды тушения (тушение растворителем, тушение
электролитами, тушение при диссоциации и ионизации молекул и т. д.). При
проведении люминесцентного анализа интенсивность свечения играет очень большую
роль. Поэтому учет тушения, изменяющего интенсивность люминесценции и
затрудняющего анализ, является крайне важным.Закон затухания люминесценции.
Закон затухания свечения после прекращения возбуждения может быть
различным у разных веществ, что часто позволяет по нему определять природу и
кинетику свечения; вместе с тем он может служить и аналитической
характеристикой. Закон затухания свечения растворов и молекулярных кристаллов
обычно достаточно хорошо выражается экспоненциальной зависимостью
(4).
где I — интенсивность свечения в момент времени t; I0 —
интенсивность свечения в момент прекращения возбуждения; t — средняя длительность
возбужденного состояния (время, в течение которого интенсивность свечения
уменьшается в е раз, т. е. в 2,7 раза). В других случаях затухание свечения
может происходить по более сложному закону. Так, например, затухание свечения
кристаллофосфоров хорошо описывается эмпирической формулой
(5)
где A, b, a — постоянные, причем обычно a<2.
1.3 Длительность возбужденного состояния молекул
После прекращения возбуждения свечение не исчезает мгновенно, а продолжается
определенный промежуток времени. Длительность возбужденного состояния у разных
соединений может существенно различаться. Она характерна для каждого вещества и
является его важной оптической характеристикой. Так, для растворов обычно t~10 — 8—10 — 9
сек. Затухание свечения кристаллофосфоров протекает по сложным законам и может
продолжаться секунды, минуты и даже часы.Таким образом, у жидких растворов t очень невелико и их
люминесценция затухает практически мгновенно. Такие свечения часто называют
флуоресценцией. При введении тех же веществ в очень вязкие среды (в желатину,
сахарные леденцы и т. д.), а также при замораживании растворов возникает
длительное свечение, продолжающееся доли секунды и даже целые секунды. Свечение
такого вида называют замедленной флуоресценцией, или фосфоресценцией. Известны
два вида замедленной флуоресценции: при одном спектр свечения совпадает со
спектром флуоресценции (a-процесс), при втором наблюдается резко отличный
спектр свечения, сдвинутый в сторону длинных волн (b-процесс).Замедленная флуоресценция обусловлена попаданием возбужденных
молекул на энергетические уровни, непосредственный переход с которых в
невозбужденное состояние не разрешен. Эти уровни называются метастабильными;
молекула может их покинуть лишь под влиянием внешних воздействий (например, при
нагревании). Возбужденные молекулы пребывают на метастабильных уровнях
значительное время, вызывая увеличение длительности послесвечения.При сложном законе затухания (например, (5)) понятие средней
длительности возбужденного состояния t уже неприменимо. В этом
случае для характеристики длительности послесвечения обычно принимают время, в
течение которого интенсивность свечения исследуемого образца уменьшается в
определенное число раз (в 100—1000 раз).1.4 Кривые термического высвечивания
У многих веществ (кристаллофосфоров, минералов, кварца и др.),
предварительно возбужденных ультрафиолетовой, рентгеновской или радиоактивной
радиацией, при нагревании возникает свечение, получившее название
термолюминесценции. Оно наблюдается при температурах, значительно меньших тех,
при которых появляется видимое температурное излучение.Термолюминесценция имеет следующее происхождение. Под действием
возбуждающей радиации электроны отрываются от ионов облучаемого вещества; часть
их непосредственно рекомбинирует с ионизованными центрами, что приводит к
возникновению кратковременного свечения кристаллофосфоров; другая часть
электронов задерживается вблизи мест нарушения периодичности кристаллической
решетки — на уровнях локализации. Освобождение электронов с мест локализации
происходит за счет тепловой энергии. Их последующая рекомбинация с
ионизованными центрами вызывает длительное свечение кристаллофосфоров.Уровни локализации могут иметь различную энергетическую глубину,
т. е. могут удерживать электроны с различной силой. Мелкие уровни освобождаются
уже при температуре жидкого азота, глубокие — при +300, +400°С. При постепенном
нагревании предварительно возбужденного фосфора последовательно освобождаются
уровни разной глубины, и интенсивность термолюминесценции то увеличивается, то
уменьшается. Кривые, характеризующие зависимость яркости свечения фосфора от
температуры, получили название кривых термического высвечивания. Они являются
важной характеристикой кристаллофосфоров и могут быть использованы для
аналитических целей.1.5 Основные закономерности свечения, используемые в
люминесцентном анализеЗакон независимости спектра люминесценции от длины волны
возбуждающего света.При возбуждении свечения различными длинами волн молекулы вещества,
поглощая кванты разной величины, попадают на различные колебательные уровни
возбужденного электронного состояния. Поэтому можно ожидать, что спектр
люминесценции будет зависеть от длины волны возбуждающего света. Однако
оказалось, что каждое вещество в конденсированном состоянии имеет совершенно
определенный спектр люминесценции, который не чувствителен к изменению длины
волны возбуждающего света.Это объясняется тем, что молекулы, перешедшие в результате
возбуждения на различные колебательные уровни возбужденного состояния (рис. 1),
успевают за время, много меньшее, чем средняя длительность возбужденного
состояния t, растратить часть колебательной энергии и образовать систему
возбужденных молекул, обладающих равновесным распределением колебательной
энергии, определяемым температурой. Из этих вполне определенных для данной
температуры состояний и происходят переходы молекул в невозбужденное состояние,
сопровождающиеся излучением. Поэтому на опыте всегда наблюдается один и гот же
спектр люминесценции, не зависящий от длины волны возбуждающего света.Независимость спектра люминесценции от длины волны возбуждающего
света позволяет на практике пользоваться для возбуждения широкими спектральными
участками. При отсутствии вторичного поглощения оказывается возможным не
обращать внимания на состав возбуждающего света, что очень сильно облегчает
проведение анализа.1.6 Закон Стокса—Ломмеля
Стоксом было сформулировано правило, согласно которому свет
люминесценции всегда имеет большую длину волны по сравнению со светом,
применявшимся для возбуждения. Однако во многих случаях правило Стокса не
выполняется. Спектры поглощения и люминесценции многих веществ частично
накладываются друг на друга. Если для возбуждения взять частоту (например, n = 530·10 — 12
сек — 1), находящуюся в области наложения спектров, то согласно
правилу Стокса должна появляться лишь та часть спектра люминесценции, которая
расположена по левую сторону от выбранной частоты. Однако в соответствии с
законом независимости спектра люминесценции от возбуждающей длины волны в
большинстве случаев наблюдается полный спектр люминесценции, имеющий целый ряд
частот, превышающих частоту возбуждающего света (заштрихованная область). Таким
образом, правило Стокса нарушается. Часть спектра люминесценции, состоящая из
лучей с частотами, большими частоты возбуждающего света, называется
антистоксовской. Ее возникновение можно объяснить наличием у излучающих молекул
помимо энергии возбуждения еще определенного запаса колебательной энергии.
Сумма энергий возбуждающего и колебательного квантов позволяет получать большие
кванты люминесценции, обусловливающие появление антистоксовской части спектра.
Ломмель уточнил правило Стокса, предложив для него следующую формулировку:
спектр излучения в целом и его максимум всегда сдвинуты по сравнению со
спектром поглощения и его максимумом в сторону длинных волн. Закон
Стокса—Ломмеля строго выполняется для очень широкого круга веществ.Сдвиг спектров люминесценции относительно спектров поглощения дает
возможность более или менее просто отфильтровывать рассеянную часть
возбуждающего света, примешивающегося к люминесценции. Это обстоятельство
широко используется в практике люминесцентного анализа.Закон Вавилова.
С. И. Вавиловым установлено, что энергетический выход
люминесценции растет пропорционально длине волны возбуждающего света, затем в
некотором спектральном интервале он остается постоянным, после чего в области
наложения спектров поглощения и люминесценции начинает быстро падать. Падение
энергетического выхода свечения происходит в антистоксовской части спектра.Легко показать, что пропорциональность энергетического выхода
длине волны возбуждающего света соответствует постоянству квантового выхода в
той же спектральной области, где в излучение всегда переходит одна и та же доля
возбуждающих световых квантов. С. И. Вавилов дал своему закону формулировку,
согласно которой люминесценция может сохранять постоянный квантовый выход, если
возбуждающая волна преобразуется в среднем в более длинную, чем она сама.
Наоборот, выход люминесценции резко уменьшается при обратном преобразовании длинных
волн в короткие. Закон Вавилова широко используется в люминесцентном анализе
при подборе оптимальных условий проведения опыта.
1.7 Правило зеркальной симметрии спектров поглощения и люминесценции
Для широкого круга веществ (растворов красителей, ряда
ароматических и многих других соединений) выполняется установленное В. Л.
Левшиным правило зеркальной симметрии спектров поглощения и излучения, согласно
которому спектры поглощения и люминесценции, изображенные в функции частот,
оказываются зеркально-симметричными относительно прямой, проходящей
перпендикулярно оси частот через точку пересечения обоих спектров, т. е.
(6)
или
(7)
Здесь nП — частота поглощаемого света; nЛ — симметричная частота
люминесценции; n0 — частота линии симметрии. При этом по оси
ординат для спектров поглощения откладываются коэффициенты поглощения a, а для спектров
люминесценции — квантовые интенсивности IКВ=I/n.Из уравнения (9) видно, что при наличии зеркальной симметрии Dn=nП — nЛ, и nП связаны линейной
зависимостью. Если откладывать по оси абсцисс nП, а по оси ординат Dn, то при строгом
выполнении правила должна получиться прямая линия.Для осуществления зеркальной симметрии необходимо выполнение двух
условий — зеркальной симметрии частот и зеркальной симметрии интенсивностей
поглощения и люминесценции в соответствующих частях спектра.Для осуществления симметрии частот необходимо, чтобы
энергетические уровни возбужденного и невозбужденного состояний были построены
одинаково. Для наличия зеркальной симметрии интенсивностей необходимо, чтобы
распределение молекул по энергетическим уровням верхней и нижней систем было
одинаковым и чтобы вероятности соответствующих излучательных и поглощательных
переходов были равны, или пропорциональны друг другу. Эти условия выполняются
лишь у части молекул. У веществ, следующих правилу зеркальной симметрии, можно
по одному из спектров (люминесценции или поглощения) без измерений установить
форму другого. Отступления от правила зеркальной симметрии могут быть
использованы для установления величины отклонений от условий его выполнения.Правило зеркальной симметрии оказывается весьма полезным при
проведении люминесцентного анализа, а также при расшифровке спектров и
установлении энергетических уровней исследуемых молекул.1.8 Виды люминесцентного анализа и характеристика его
особенностейЛюминесцентным анализом называется обнаружение и исследование
различных объектов с помощью явлений люминесценции. Наиболее важной задачей
люминесцентного анализа является определение химического состава исследуемых
веществ и установление процентного содержания в них отдельных компонентов.
Анализ такого вида носит соответственно название качественного и
количественного химического люминесцентного анализа.Качественный химический люминесцентный анализ основан на том, что
люминесцентные свойства являются характерным признаком излучающего вещества,
тесно связанным с его составом, общим состоянием и структурой его молекул.Количественный химический люминесцентный анализ основан на
использовании определенной зависимости между интенсивностью люминесценции и
концентрацией люминесцентного вещества. В большинстве случаев условия анализа
подбираются так, чтобы осуществлялась пропорциональность между интенсивностью
свечения и концентрацией вещества. Однако такая зависимость имеет место лишь в
случаях, когда концентрации невелики. При высоких концентрациях определяемого
вещества для осуществления анализа приходится тем или иным способом учитывать
сложную зависимость интенсивности свечения от концентрации.К люминесцентному анализу относится также изучение структуры и
колебательных частот молекул по спектрам излучения, создающее фундамент для
качественного люминесцентного анализа.Чисто химические задачи не исчерпывают возможностей
люминесцентного анализа. С его помощью можно обнаруживать и выявлять различные
объекты и их детали, изучение которых оказывается невозможным при обычных
условиях наблюдения и освещения. Люминесцентный анализ такого рода получил
название люминесцентного анализа обнаружения или сортового люминесцентного
анализа.В то время как при химическом и эмиссионном спектральном анализе
анализируемые вещества разлагаются, при люминесцентном анализе они, как
правило, не подвергаются изменениям и их можно использовать в дальнейшей
работе. Это преимущество люминесцентного анализа особенно существенно при
исследовании трудно синтезируемых уникальных веществ, получаемых в ничтожных
количествах. В отдельных случаях возбуждения люминесценции коротковолновыми
ультрафиолетовыми лучами в веществе могут происходить фотохимические
превращения. Однако соответствующим подбором условий опыта эти трудности обычно
могут быть обойдены.Перечисленные свойства люминесцентного анализа дают представление
о его исключительных возможностях, в определенных отношениях значительно
превосходящих возможности других видов анализа. Однако следует отметить, что
необычайно высокая чувствительность люминесцентного анализа одновременно
создает и серьезные трудности его проведения, существенно ограничивая области
его применения. Присутствие в образце даже ничтожных количеств люминесцирующих
примесей обусловливает появление нового свечения, которое накладывается на
люминесценцию основного вещества, искажая как спектральный состав, так и
интенсивность его излучения. Поэтому значительные успехи в применении
люминесцентного анализа могли быть достигнуты лишь на основе всестороннего
развития учения о люминесценции в целом, после того как были установлены общие
законы свечения и накоплен большой материал о люминесцентных свойствах
различных классов соединений.Наиболее распространенным и хорошо разработанным является
люминесцентный анализ, основанный на возбуждении фотолюминесценции. При анализе
кристаллических неорганических веществ (минералов, алмазов и др.) применяют
катодное и рентгеновское возбуждения. В отдельных случаях в аналитических целях
используют явления хемилюминесценции и радиолюминесценции.1.9 Рентгенофлуоресцентный метод
Метод
основан на зависимости интенсивности рентгеновской флуоресценции от
концентрации элемента в образце. При облучении образца мощным потоком излучения
рентгеновской трубки возникает характеристическое флуоресцентное излучение
атомов, которое пропорционально их концентрации в образце. Излучение
разлагается в спектр при помощи кристалл-анализаторов, далее с помощью
детекторов и счетной электроники измеряется его интенсивность. Математическая
обработка спектра позволяет проводить количественный и качественный анализ.1.10 Рентгеновская флуоресценция
Когда
атомы образца облучаются фотонами с высокой энергией — возбуждающим первичным
излучением рентгеновской трубки, это вызывает испускание электронов. Электроны
покидают атом. Как следствие, в одной или более электронных орбиталях
образуются «дырки» — вакансии, благодаря чему атомы переходят в
возбужденное состояние, т.е. становятся нестабильны. Через миллионные доли
секунды атомы возвращаются к стабильному состоянию когда вакансии во внутренних
орбиталях заполняются электронами из внешних орбиталей. Такой переход
сопровождается испусканием энергии в виде вторичного фотона — этот феномен и
называется «флуоресценция«». Энергия вторичного фотона находится в
диапазоне энергий рентгеновского излучения, которое располагается в спектре
электромагнитных колебаний между ультрафиолетом и гамма-излучением.

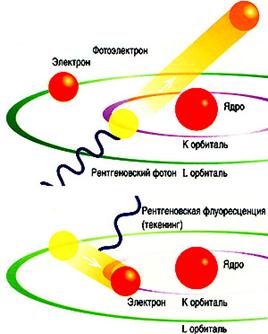
Различные
электронные орбитали обозначаются K, L, M и т.д., где К – орбиталь, ближайшая к
ядру. Каждой орбитали электрона в атоме каждого элемента соответствует
собственный энергетический уровень. Энергия испускаемого вторичного фотона
определяется разницей между энергией начальной и конечной орбиталей, между
которыми произошел переход электрона.
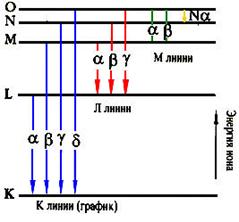
Длина
волны испускаемого фотона связана с энергией формулой E = E1-E2
= hc/l , где E1 и E2 – энергии орбиталей, между которыми
произошел переход электрона, h – постоянная Планка, с — скорость света, l —
длина волны испускаемого(вторичного) фотона. Таким образом, длина волны
флуоресценции является индивидуальной характеристикой каждого элемента и
называется характеристической флуоресценцией. В то же время интенсивность
(число фотонов, поступающих за единицу времени) пропорциональна концентрации
(количеству атомов) соответствующего элемента. Это дает возможность элементного
анализа вещества: определение количества атомов каждого элемента, входящего в
состав образца.ГЛАВА 2. ОБЛАСТИ ПРИМЕНЕНИЯ ФЛУОМЕТРИИ В АНАЛИЗЕ ОБЪЕКТОВ
ОКРУЖАЮЩЕЙ СРЕДЫСегодня
люминесцентный метод анализа охватывает широкий круг методов определения
разнообразных объектов от простых ионов и молекул до высокомолекулярных
соединений и биологических объектов. Детектируется люминесценция самого объекта
или его производных, возможно также использование изменения люминесценции
специфичных агентов. Для сложных проб люминесцентное детектирование сочетается
с химическим разделением (хроматография, электрофорез) или с биологическим
выделением (иммуноанализ, метод полимеразной цепной реакции — ПЦР).2.1 Важные для химического анализа свойства
люминесценции1.
Возможность различения объектов по способам возбуждения люминесценции и его
параметрам, например:§ фотолюминесценция (спектр
возбуждения)§ хемилюминесценция
(параметры реакции)§ перенос энергии (характер
донорно-акцепторного взаимодействия и условия возбуждения донора).2.
Возможность различения объектов по параметрам излучения:§ спектр излучения
§ кинетика высвечивания
(при импульсном возбуждении фотолюминесценции или при импульсном смешении хемилюминесцентных
реагентов)3.
Возможность регистрации люминесценции в отсутствии иных свечений в спектральном
диапазоне регистрации.4.
Интенсивность люминесценции прямо пропорциональна интенсивности возбуждения.5.
Параметры люминесценции молекул и ионов в конденсированной среде, как правило,
сильно зависят от свойств матрицы и, в первую очередь, ближайшего окружения.Благодаря
этим особенностям, достигнуты очень низкие пределы определения (до 1 ppt и
ниже) и высокая селективность (например, разделение ПАУ).Выбор
оптимальных условий градуирования методик рентгенофлуоресцентного анализа (РФА)
фильтров, нагруженных атмосферными аэрозолямиДля
определения тяжелых металлов в атмосферных аэрозолях, собранных на фильтр,
метод РФА является одним из самых перспективных. Однако градуирование методик
РФА и контроль правильности результатов анализа затруднен из-за отсутствия
отечественных стандартных образцов (СО) состава аэрозолей. Решение этой
проблемы видится в создании синтетических СО и изыскании способов учета различия
физико-химических свойств СО и реальных проб.Испытано два
приема приготовления СО: осаждение порошкового препарата на фильтр; введение
порошка в раствор полимера и получение из смеси тонкой пленки. В качестве
носителя частиц аэрозоля использован материал ГСО почв с добавками соединений
тяжелых металлов. Первый прием оказался мало пригодным из-за потерь
определяемых компонентов и неоднородности распределения порошка по фильтру: при
нагрузке менее 5 мкг/см2 (соответствует пробам аэрозолей) погрешность
получения СО характеризуется относительным стандартным отклонением, равным 0,3.
Для пленочных СО эта погрешность, обусловленная неоднородностью пленки по
составу и толщине, не превышает 0,07.Изучено
влияние крупности D частиц порошкового препарата в пленочном образце на
интенсивность Ii флуоресценции в области средних и коротких длин
волн. Установлено, что для пленок на основе мономинеральной фракции при
уменьшении D от 60 до 5 мкм Ii возрастает на 60 %. Для смеси
минералов это изменение не превышает 30 %, для ГСО почв зависимость Ii
=f(D) выражена слабо. Рекомендовано порошок, используемый при изготовлении СО
доизмельчать со спиртом в агатовой ступке в течение 3 ч.Для учета
различия физико-химических свойств пленочных СО и реальных проб аэрозолей испытаны
способы РФА, использующие в качестве корректирующих параметров интенсивность I
рассеянного излучения, измеренного на различных участках рентгеновского спектра
и интенсивность Iп флуоресценции атомов подложки, помещенной под
анализируемый образец. Даны рекомендации по выбору оптимальных условий
градуирования методики РФА аэрозолей.2.2 Проблема ПАУ и их содержание в природных
средах КузбассаПАУ
(полициклические ароматические углеводороды) образуются при неполном сгорании
органических веществ. Воздействие ПАУ на человека происходит при вдыхании
загрязненного воздуха, табачного дыма, приеме загрязненной воды и пищи, а также
при попадании на кожу сажи, смолы, нефти. Долгое время предполагалось, что ПАУ
представляют только потенциальную опасность для здоровья человека; теперь
установлено, что многие представители этого класса являются канцерогенами и
(или) мутагенами. Из 16 соединений этой группы, подлежащих определению,
наиболее распространенным является нафталин, а наиболее токсичным
3,4-бенз(а)пирен (его ПДК в воде составляет 0.005 мкг/л, в почве 0.02 мкг/л, в
воздухе 0.1 мкг/100м3). Из-за высокой токсичности 3,4-бенз(а)пирена
его определение входит в программы глобального мониторинга загрязнений ОС.Поступление
ПАУ в окружающую среду обусловлено, в основном, сжиганием каменного угля,
работой мусоросжигающих печей и двигателей на бензине или дизельном топливе.
Много их накапливается в атмосфере при лесных пожарах, в результате
вулканической деятельности.По
данным постов наблюдения Гидрометеослужбы в Кузбассе за 1996 год высокое
загрязнение атмосферы 3,4-бенз(а)пиреном наблюдалось в городах Кемерово,
Новокузнецк, Прокопьевск. В частности, в Кемерово среднегодовая концентрация
3,4-бенз(а)пирена превышала ПДК в 5,4 раза. Наибольшее загрязнение этой примесью
отмечается в правобережной части города (Кировский район), находящейся под
влиянием выбросов промышленных предприятий Заводского и Кировского районов. На
посту данного района средняя концентрация составила 7,3 ПДК; максимальная за
год по Кузбассу отмечена здесь же (20,4 ПДК). Нафталин обнаружен не был.
Наибольшее загрязнение наблюдается в период отопительного сезона. В 1995 г.
было отмечено превышение ПДК в 7,9 раз, в 1990 г. — в 3,9 раз (данные по
Кировскому району). В Новокузнецке наибольшее загрязнение данным ПАУ
наблюдается в центре города (до 9,7 ПДК), в целом по городу средняя
концентрация составляет 4,3 ПДК. Таким образом, основные источники загрязнения
3,4-бенз(а)пиреном в Кузбассе — крупнейшие металлургические предприятия,
котельные и ГРЭС, отопительные печи частного сектора и транспорт.Сведения
о содержании ПАУ в воде и почве крайне ограничены. Для определения ПАУ
международными стандартами рекомендуются следующие методы: КГХ\МС, ВЭЖХ\УФ
и/или ВЭЖХ с флуоресцентным детектированием. В работе приводятся данные по
отработке методики определения нафталина и 3,4-бенз(а)пирена в воде на
жидкостном хроматографе фирмы Varian с использованием УФ детектора на диодной
матрице и флуоресцентного детектора.Применение спектрофлуориметра Fluorolog
FL3-22 для определения типов нефтепродуктов в окружающей среде по спектрам их
люминесценции.На сегодняшний день существует несколько
методов для качественного и количественного определения нефтепродуктов в
различных компонентах окружающей среды, каждый из которых имеет свои
преимущества и недостатки. К сожалению, только немногие из этих методов
(например, газовая хроматография) дают возможность определить конкретный тип
нефтепродукта, что важно при определении источника загрязнения.В докладе будет описано применение спектрофлуориметра
Fluorolog FL3-22 (Jobin Yvon Inc., Германия), позволяющего получать спектры
люминесценции растворов при комнатной температуре, для исследования различных
типов нефтепродуктов (дизельного топлива, масел, мазута, битума). Проведенные
эксперименты выявили возможность определения типа нефтепродукта по спектрам
излучения и поглощения их гексановых растворов. Преимущества данного метода —
полная сохранность вещества в процессе анализа, отсутствие температурного
воздействия на образец, относительно небольшая продолжительность исследования –
могут сделать его альтернативой методу газовой хроматографии в области
качественного анализа нефтепродуктов — загрязнителей окружающей среды.ГЛАВА 3. СОВРЕМЕННОЕ ОБОРУДОВАНИЕ
Применимость
к разнообразным объектам, высокая чувствительность и селективность методов
люминесцентного анализа сочетаются с возможностью реализации их на относительно
недорогой и компактной аппаратуре.3.1 PHYTO-PAM
Анализатор фитопланктона

Флуориметр Walz PHYTO-PAM – это четырехволновой измеритель
флуоресценции хлорофилла для ультрачувствительного измерения содержания
хлорофилла в фотосинтезирующих объектах, состава и фотосинтетической активности
образцов фитопланктона в поверхностных водах естественной среды обитания, а
также для работы с такими образцами как бентос, перифитон (microphytobenthos,
periphyton) и другими.Уникальными особенностями прибора являются:
·
возможность
дифференциации между зелеными водорослями, диатомовыми и цианобактериями·
возможность
измерений эффективности квантового выхода и скорости электронного транспорта
(electron transport rate, ETR)·
автоматическая
регистрация кривых светового отклика (light response curves) значений выхода и
электронного транспорта·
специальное
программное обеспечение PhytoWin для контроля системы, сбора данных и их
анализа с помощью компьютераДоступны три альтернативных варианта исполнения флуориметра
PHYTO-PAM, оснащенных излучающими и детектирующими модулями различного типа:PHYTO-PAM I — для работы в лаборатории с использованием
стандартных кювет размером 10×10 мм. Комплектуется оптическим модулем ED — 101US
и отдельными массивами светоизлучающих элементов LED для измерения и для
освещения образцов (Actinic Light). Эта система рекомендуется для всего спектра
исследований благодаря хорошо отъюстированной оптике.PHYTO-PAM II — для работы в полевых условиях (может применяться и
в условиях лаборатории) с использованием 15 мм кювет в универсальном модуле
PHYTO-ED, в который интегрированы все оптические и электронные компоненты для
минитюаризации прибора.PHYTO-PAM III — для работы с такими образцами как бентос,
перифитон (microphytobenthos и periphyton) и другими, комплектуется специальным
оптоволоконным измерительным модулем PHYTO-EDF.Доступные аксессуары:
·
миниатюрная
магнитная мешалка (PHYTO-MS) (для PHYTO-PAM I)·
модуль
контроля температуры (US-T) (для PHYTO-PAM I)·
мешалка (WATER-S) (для PHYTO-PAM II)·
сферический
квантовый микросенсор (US-SQS/B) (для PHYTO-ПАМ I и PHYTO-PAM II)Технические характеристики:
Система Walz PHYTO-PAM I для работы в лаборатории
Контрольный блок PHYTO-C
Микроконтроллер: RISC-процессор, интерфейс: управляющий компьютер
типа IBM PC под управлением MS Windows, ПО PhytoWin. Интерфейс для
подсоединения к компьютеру типа RS 232 (19200). Встроенная клавиатура.
Встроенный цифровой дисплей. Вывод данных: на экран и на печать через
компьютер. вывод аналоговых данных флуоресценции по четырем каналам (0-5
Вольт). Источник питания: встроенная перезаряжаемая свинцовая батарея 12 Вольт
/ 7,2 Ач; зарядное устройство для батареи MINI-PAM/L (100 — 240 Вольт).
Потребление: 350 mA; при включении всех светодиодных источниках света
максимально до 800 mA. Размеры (Ш х В х Д): 31 x 16 x 33,5 см. Вес: 6,1 кг.Программное обеспечение PhytoWin.
Семь программных окон для вывода и анализа данных. Деконволюция
информации по флуоресценции для зеленых водорослей, диатом и цианобактерий (на
основе записанных заранее референсных спектров). Вывод данных: полный отчет
включая все измеренные параметры и установки измерений; возможность экспорта в
другие программы. Графический вывод световых кривых, и кривых зависимости ETR
от PAR.Оптический блок ED — 101US/MP
Алюминиевый корпус, кюветное отделение 10 x 10 мм, материал кюветы
– стекло. Порты для подсоединения измерительного светодиодного блока и
детекторного фотоумножительного блока.Три дополнительных оптических порта для подсоединения источника
актиничного света (опция), миниатюрной магнитной мешалки (опция);
светонепроницаемого экрана с инжекционным отверстием. В комплекте
штатив-подставка ST — 101. Вес 850 г.Измерительный светодиодный блок PHYTO-ML
Светодиодный массив состоящий из 25 светоизмерительных светодиодов
с максимумом при длинах волн 470, 520, 645 и 665 нм; 12 светодиодов актиничного
света с максимумом при длине волны 655 нм (максимальная интенсивность 600 µmol
quanta m — 2s — 1 PAR), световодный конус сужающий луч до диаметра в 13 мм; фильтр
типа «short-pass» (λ < 695 нм) на выходе конуса; алюминиевый корпус
темного цвета анодированный. размеры диаметр 59 мм, длина 190 мм. Вес: 630 г
включая кабель длиной 1,5 м.Источник актиничного света PHYTO-AL
Светодиодный массив состоящий из 37 светодиодов актиничного света
с максимумом при длине волны 655 нм, (максимальная интенсивность 2000 µmol
quanta ms PAR), световодный конус сужающий луч до диаметра в 13 мм; фильтр типа
«short-pass» (λ < 695 нм) на выходе конуса; алюминиевый корпус темного
цвета анодированный. размеры диаметр 59 мм, длина 190 мм. Вес: 600 г включая
кабель длиной 1,5 м.Детекторно-фотоумножительный модуль PM — 101P
Алюминиевый корпус, адаптер для закрепления на оптическом блоке.
Детекция сигнала: минифотоумножитель с высокой «красной»
интенсивностью (модель H6779-01, Hamamatsu). Детекторный фильтр: комбинация
трех фильтров с длиной волны пропускания свыше 710 нм, оптимизированных под
низкий уровень фонового сигнала.Размеры (Д х Ш х В): 100 x 66 x 108 мм.
Вес: 490 г (включая кабель длиной 1,5 м).
Штатив-подставка ST — 101
Утяжеленная основа (39,5 x 30 x 2 см), вертикальный штатив
диаметром 15 мм, высотой 76,5 см, вес 2,8 кг.Система Walz PHYTO-PAM II для работы в полевых условиях PHYTO-ED
Эмиттерно-детекторный блок PHYTO-ED
Дизайн: металлический корпус с кабелями подсоединения к
управляющему модулю PHYTO-C; кюветное отделение под круглые кюветы диаметром 15
мм; материал кювет – кварц. В корпус интегрированы светодиодные массивы
(измерительный и светодиодный массив актиничного света / насыщающих световых
импульсов), а также детектор с фотоумножителем и предусилитель.Измерительный светодиодный массив: 18 светодиодов для
модулируемого измерительного света (470, 520, 645 и 665 нм), свет фокусируется
в нижней части кварцевой кюветы. Каждый светодиод оснащен индивидуальным
фильтром типа «short-pass» (λ < 695 нм).Светодиодный массив актиничного света: 16 светодиодов для
актиничного облучения и насыщающих световых импульсов, с максимумом при 655 нм,
свет фокусируется в нижней части кварцевой кюветы. Интенсивность актиничного
облучения: до 2000 µmol quanta m — 2s — 1 of PAR. Интенсивность насыщающих
импульсов: до 4000 µmol quanta m — 2s — 1.Детекция сигнала: детектор-фотоумножитель — фотосенсорный модуль
(H — 6779-01, Hamamatsu) с высокой «красной» интенсивностью. Импульсный
предусилитель, детекция флуоресценции при длинах волн > 710 нм; оптимизация
под низкий уровень фонового сигнала.Размеры (Д х Ш х В): 115 x 90 x 80 мм. Вес: 600 г, включая кабель
длиной 60 см.Система Walz PHYTO-PAM III для измерений на поверхностях PHYTO-EDF
Эмиттерно-детекторный оптоволоконный модуль PHYTO-EDF
Дизайн: металлический корпус с кабелями подсоединения к
управляющему модулю PHYTO-C;светодиоды измерительные и светодиоды актиничного света /
насыщающих световых импульсов, соединенные с миниатюрными оптоволоконными
волноводами (9 шт.), интегрированный детектор с фотоумножителем и
предусилитель.Размеры (Д х Ш х В): 115 x 90 x 95 мм. Вес: 600 г, включая кабель
длиной 60 см.Измерительные светодиоды: 4 светодиода для модулируемого
измерительного света (470, 520, 645 и 665 нм), фокусируются миниатюрными
коллиматорными линзами, оснащаются четырьмя индивидуальными фильтрами типа
«short-pass» (λ < 695 нм) на входе 1 мм индивидуальных пластиковых
оптоволоконных волноводов.Светодиоды актиничного света / насыщающих световых импульсов: 4
светодиода с максимумом при 655 нм, фокусируются миниатюрными коллиматорными
линзами, оснащаются четырьмя индивидуальными фильтрами типа «short-pass»
(λ < 695 нм) на входе 1 мм индивидуальных пластиковых оптоволоконных
волноводов. Интенсивность актиничного света до 1300 µmol quanta m — 2s — 1 PAR);
интенсивность насыщающих световых импульсов до 2600 µmol quanta m — 2s — 1.Детекция сигнала: детектор-фотоумножитель — фотосенсорный модуль
(H — 6779-01, Hamamatsu) с высокой «красной» интенсивностью. Импульсный
предусилитель, детекция флуоресценции при длинах волн > 710 нм; оптимизация
под низкий уровень фонового сигнала.Оптоволоконные волноводы: 8 волноводов пластиковых диаметром 1 мм
подсоединяются к коннекторам измерительного и актиничного света на верхней
панели эмиттерно-детекторного модуля. Центральный волновод диаметром 1,5 мм
подсоединяется к коннектору детектора. Длина волновода 105 см. Объединенный
конец со специальным смесительным световым элементом-окончанием диаметром 4 мм,
длина 50 см.Специальная подставка: утяжеленное основание (39,5 x 30 x 2);
штатив диаметром 15 мм, высота 76.5 см, вес 2,8 кг; со специальным держателем
для окончания оптоволоконных волноводов, темновой бокс для защиты образца от
внешнего светового облучения.3.2 АЛИЗАТОР ФЛЮОРАТ 02 2М
Анализатор ФЛЮОРАТ 02 2М предназначен для
измерения массовой концентрации неорганических и органических примесей в воде,
а также воздухе, почве, технических материалах, пищевых продуктах после
переведения примесей в раствор. Применяется для аналитического контроля объектов
окружающей среды, санитарного контроля и контроля технологических процессов.
Анализатор Флюорат может быть использован в качестве детектора в хроматографии.Анализатор ФЛЮОРАТ 02 2М используется при
выполнении рутинных измерений объектов, для которых предварительно установлены
спектральные характеристики люминесценции. Селекция световых потоков
осуществляется специально подобранными светофильтрами. В качестве источника
света используется импульсная ксеноновая лампа высокого давления, обеспечивающая
достаточные световые потоки во всем спектральном диапазоне оптических методов —
от жесткого ультрафиолета до красной границы видимого света. Основной режим
работы анализатора — флуориметр. Флюорат может также работать как фотометр или
хемилюминометр. В кюветное отделение можно устанавливать кюветы 10х10 мм для
флуориметрии и 10х20, 10х40 мм для фотометрии. Анализатор работает от сети
переменного тока или от батареи 12 В. Это позволяет использовать его в составе
передвижных лабораторий. На приборе реализован метод абсорбционной фотометрии.
Флюорат 2 2М может применяться в качестве внешнего флуориметрического детектора
систем ВЭЖХ, капиллярного электрофореза и т.п.

ОТЛИЧИТЕЛЬНЫЕ
ОСОБЕННОСТИ:·
низкие
пределы определения·
высокая
селективность·
широкая
номенклатура определяемых показателей·
сокращение
времени анализа и расхода реактивов·
сохранение
градуировок в энергонезависимой памяти·
многофункциональность
(работает как флуориметр, хемилюминометр, прибор для измерения фосфоресценции,
фотометр, нефелометр; с приставками (модель 2М) реализует криолюминесцентный
анализ, также работает как флуориметрический детектор для ВЭЖХ-системы)В
основу работы анализатора положен фотометрический, флуориметрический и
хемилюминесцентный методы измерения массовой концентрации органических и
неорганических веществ в области спектра 200 — 650 нм.Анализатор
Флюорат 2 2M комплектуется наборами для анализа интересующих пользователя
компонентов. В набор входят текст и сертификат методики, кювета, светофильтры,
стандартный образец, специфические красители (если используются). Поскольку
расход реактивов при анализе на приборе чрезвычайно низок, красителей, как
правило, достаточно для нескольких лет интенсивной работы.Области
применения Флюорат 02 2М:Экологические
исследования.·
Экспресс-анализ
воды водоемов и водотоков на содержание поллютантов.·
Скрининговые
обследования акваторий, имеющих риск загрязнения нефтепродуктами.·
Мониторинговые
исследования содержания поллютантов в водоемах.·
Контроль
загрязненности почв и грунтов нефтепродуктами и тяжелыми металлами.Санитарные
исследования.·
Контроль
содержания токсичных веществ и соединений в питьевых и сточных водах.·
Контроль
загрязнения воздушной среды аэрозолями и летучими веществами (после перевода
проб в жидкую фазу).Геология.
·
Исследования
гидрогеологических процессов методом «флуоресцирующей метки».Технология.
·
Контроль
содержания остаточных количеств нефтепродуктов в жидком кислороде. Контроль
чистоты технологических растворов.Медицина.
·
Рутинные
анализы биологических сред.Контроль
пищевых продуктов на содержание витаминов В1, В2, С.Анализ
ПАУ. В комплекте с системой ВЭЖХ Анализатор Флюорат 2 2M обеспечивает
выполнение измерений содержания без/а/пирена и других ПАУ в воздушной среде,
водах (природная, питьевая, сточная), почве, пищевых продуктах.3.3 АНАЛИЗАТОР ФЛЮОРАТ 02 3М
Анализатор Флюорат 02 3М является базовой
моделью анализаторов типа Флюорат 2, предназначенной для определения массовой
концентрации неорганических и органических примесей в воде, воздухе, почве,
технических материалах, пищевых продуктах после переведения примесей в раствор.
Анализатор снабжен жидкокристаллическим дисплеем.Упрощенная
модель фильтрового флуориметра, предназначена для выполнения рутинных измерений
объектов для которых предварительно установлены спектральные характеристики
фотолюминесценции. Селекция световых потоков осуществляется специально
подобранными светофильтрами. В качестве источника света используется импульсная
ксеноновая лампа высокого давления, обеспечивающая достаточные световые потоки
во всем спектральном диапазоне оптических методов — от жесткого ультрафиолета
до красной границы видимого света . Основной режим работы анализатора —
флуориметр. Анализатор Флюорат 2 3М может также работать как фотометр или
хемилюминометр. В кюветное отделение можно устанавливать кюветы 10х10 мм для
флуориметрии и 10х20, 10х40 мм для фотометрии. Флюорат работает от сети
переменного тока или от батареи 12 В. Это позволяет использовать его в составе
передвижных лабораторий. Возможно измерение методами флуоресценции или
абсорбционной фотометрии.

Отличительные
особенности Флюорат 2 3М:·
низкие
пределы определения·
высокая
селективность·
широкая
номенклатура определяемых показателей·
сокращение
времени анализа и расхода реактивов·
сохранение
градуировок в энергонезависимой памяти·
многофункциональность
(Флюорат работает как флуориметр, хемилюминометр, прибор для измерения
фосфоресценции, фотометр, нефелометр)Технические
характеристики:
| Время измерения |
не более — 16 с |
| Используемые типы кювет — К10, К20, К40 |
на пробы, |
| Объем анализируемой пробы (в стандартной кювете К10) |
до — 3 см3 |
| Предел допускаемого значения абсолютной погрешности при измерении коэффициента пропускания образцов в диапазоне 10 — 90 % |
2 % |
|
Предел |
0,004+0,10*С |
| Рабочий спектральный диапазон (канал возбуждения и пропускания) |
200 — 900 нм |
| Рабочий спектральный диапазон (канал регистрации) |
250 — 900 нм |
| Температура окружающего воздуха |
10 — 35 °C |
| Средний срок службы |
не менее — 5 лет |
| Средняя наработка на отказ |
не менее — 1000 ч |
| Габариты | не более — 330*300*120 мм |
| Масса | не более — 8 кг |
| Питание | 220 В |
| Питание от автономного источника |
12 В |
| Потребляемая мощность |
не более — 36 Вт |
| Частота тока | 50 Гц |
ОБЛАСТИ
ПРИМЕНЕНИЯ:
Экологические
исследования.
·
Экспресс-анализ
воды водоемов и водотоков на содержание поллютантов.
·
Скрининговые
обследования акваторий, имеющих риск загрязнения нефтепродуктами.
·
Мониторинговые
исследования содержания поллютантов в водоемах.
·
Контроль
загрязненности почв и грунтов нефтепродуктами и тяжелыми металлами.
Санитарные
исследования.
·
Контроль
содержания токсичных веществ и соединений в питьевых и сточных водах.
·
Контроль
загрязнения воздушной среды аэрозолями и летучими веществами (после перевода
проб в жидкую фазу).
Геология.
·
Исследования
гидрогеологических процессов методом «флуоресцирующей метки».
Технология.
·
Контроль
содержания остаточных количеств нефтепродуктов в жидком кислороде. Контроль
чистоты технологических растворов.
Медицина.
·
Рутинные
анализы биологических сред.
Контроль
пищевых продуктов на содержание витаминов В1, В2, С.
Анализ
ПАУ. Флюорат 2 3М в комплекте с системой ВЭЖХ обеспечивает выполнение измерений
содержания без/а/пирена и других ПАУ в воздушной среде, водах (природная,
питьевая, сточная), почве, пищевых продуктах.
3.4 АНАЛИЗАТОР ФЛЮОРАТ 02-ПАНОРАМА
Анализатор
Флюорат 02-Панорама предназначен для широкого круга научных и методических
исследований спектрально-временных характеристик люминесценции самых
разнообразных объектов: растворы; твёрдые образцы, в том числе замороженные до
температуры жидкого азота; оптические стёкла; порошки.
Для
анализатора Флюорат разработана гамма приставок, позволяющих проводить
измерения вне кюветного отделения прибора. Вместе с тем, прибор аттестован как
анализатор Флюорат 02, что позволяет проводить измерения массовой концентрации
веществ в соответствии с утверждёнными методиками (кроме хрома и урана).
Имеется модификация прибора являющаяся спектрофлуориметрическим детектором для
ВЭЖХ. Компьютерное программное обеспечение обеспечивает управление прибором во
время проведения измерений и позволяет проводить обработку результатов.

ДОСТОИНСТВА
АНАЛИЗАТОРА:
·
наличие
монохроматоров в каналах возбуждения и регистрации люминесценции
·
Многофункциональность
прибора
·
широкий
выбор дополнительных приставок для измерений вне кюветного отделения
·
Программное
обеспечение поставляется без дополнительной оплаты.
·
Реализованы
режимы хроматографических и спектральных измерений, измерений кинетики
затухания люминесценции.
·
Использование
в качестве спектрофлюориметрического детектора для микроколоночной ВЭЖХ с
программируемой перестройкой длины волны во время процесса хроматографического
разделения.
·
Возможность
сканирования по каждому из монохроматоров как независимо, так и в режимах
синхронного, асинхронного и двумерного спектрального сканирования.
·
Измерение
кинетики фосфоресценции с шагом 0,05 мкс до 7000 мкс.
Распространенные
приложения анализатора Флюорат 02 Панорама:
·
Спектрофлуориметрическое
детектирование в HPLC:
ПАУ, микотоксины, нитрозамины, аминокислоты, витамины, гормоны
·
Спектрально-кинетические
исследования материалов и процессов
·
Спектрофлуориметрическое
детектирование в иммуноанализе и ПЦР (с микропланшетной приставкой)
·
Трехмерное
и четырехмерное распознавание образов (идентификация подлинности)
Технические
характеристики:
| Габариты анализатора |
не более — 400*355*150 мм |
| Объем анализируемой пробы (в стандартной кювете К10) |
3 мл |
| Отношение сигнал/шум для комбинационного рассеяния воды на длине волны возбуждения 350 нм (регистрация 400 нм) при постоянной времени 2с., для приборов с разрешением 15 нм не менее |
200 |
| Отношение сигнал/шум для комбинационного рассеяния воды на длине волны возбуждения 350 нм (регистрация 400 нм) при постоянной времени 2с., для приборов с разрешением 8 нм не менее |
100 |
| Погрешность установки монохроматоров, не более |
3 нм |
| Предел допускаемого значения абсолютной погрешности при измерении коэффициента пропускания образцов в диапазоне 10 — 90 % |
2 % |
|
Предел |
0,004+0,10*С |
| Разрядность применяемого АЦП |
16 |
| Спектральное разрешение монохроматоров для спектральных применений |
8 нм |
| Спектральное разрешение монохроматоров для хроматографических применений |
15 нм |
| Спектральный диапазон в каналах возбуждения люминесценции и фотометрии |
210 — 840 нм |
| Спектральный диапазон в каналах возбуждения люминесценции и фотометрии (по специальному заказу) |
210 — 840 нм |
| Спектральный диапазон в канале люминесценции |
210 — 690 нм |
| Спектральный диапазон в канале люминесценции (по специальному заказу) |
210 — 840 нм |
| Спектральный диапазон в канале пропускания |
210 — 840 нм |
| Масса | 13 кг |
| Питание | 110 — 220 В |
| Потребляемая мощность |
не более — 40 Вт |
| Частота тока |
50/60 Гц |
ОБЛАСТИ
ПРИМЕНЕНИЯ:
Анализатор
Флюорат применяется для аналитического контроля объектов окружающей среды,
санитарного контроля и контроля технологических процессов.
Экологические
исследования. Анализ спектральных характеристик, растворенных/диспергированных
в водных средах нефтепродуктов, идентификация источников загрязнения
нефтепродуктами акваторий портов, рек и водоемов. Исследования процессов
биодеградации нефтепродуктов в природных водоемах вод воздействием внешних
факторов. Исследования биопродуктивности водоемов по флуоресценции
хлорофилла-А.
Научные
исследования. Измерение спектральных характеристик свечения (спектры
возбуждения, фотолюминесценции, синхронные спектры), определение времени
затухания фосфоресценции. Исследования органических и неорганических
люминесцирующих веществ, люминесцентных меток, внедрённых в биологические
объекты.
Медицинские
исследования. Исследования свечения биопрепаратов, бактерий, вирусов, в т.ч. с
возможностью использования ПЦР-технологии (с приставкой МИКРОСКАН).
Технология.
Контроль спектральных характеристик бумаги, в т.ч. используемой для печатания
банкнот и ценных бумаг. Анализ спектральной чистоты люминофоров, иных
люминесцирующих порошков.
Геология.
Исследования гидрогеологических процессов методом «флуоресцирующей
метки».
Судебная
экспертиза. Анализ спектральных характеристик чернил, бумаги и т.п. объектов).
ЛИТЕРАТУРА
1.
Основы
аналитической химии, в 2 кн. Кн.2 Методы химического анализа Ю.А.Золотов, Е.Н.
Дорохова, В.И. Фадеева и др. /Под ред. Ю.А. Золотова 3-е изд., перераб. и доп.-
М., Высшая шк., 2004. – 503 с.
2.
Москвин
А.В. «Катодолюминесценция» 1949г.
3.
Антонов-Романовский
В.В. «Оптика и спектроскопия» 1957г.
4.
Степанов
Б.И. «Классификация вторичного свечения» 1959г.
5.
Принсгейм
П. «Флюоресценция и фосфоренценция» 1951г.
6.
Левшин
В.Л. «Фотолюминесценция жидких и твердых веществ» 1951г.
7.
Зайдель
А.Н., Атомно-флуоресцентный анализ. Физические основы метода, М., 1980 – 356 с.
8.
Алемасова
А.С., Рокун А.Н., Шевчук И.А. Аналитическая атомно-абсорбционная спектроскопия.
Севастополь: Вебер, 2003. — 327 с.
9.
Брицке
М.Э. Атомно-абсорбционный спектрохимический анализ. М.: Химия,1982, — 224 с.
10.
Лурье
Ю.Ю. Аналитическая химия промышленных сточных вод. М.: Химия, 1984. — 448 с.
11.
Львов
Б.В. Атомно-абсорбционный спектральный анализ. М.: Наука, 1966. — 392 с.
12.
Пупышев
А.А. Практический курс атомно-абсорбционного анализа: Курс лекций.
Екатеринбург: ГОУ ВПО УГТУ-УПИ, 2003. — 442 с.
13.
Славин
У. Атомно-абсорбционная спектроскопия. Л.:Химия, 1971. 269с.
14.
Хавезов
и, Цалев Д. Атомно-абсорбционный анализ. Л.: Химия, 1983.
15.
Николайчук
Н.В., Евстафьева С.А., Смагунова А.Н., Коржова Е.Н. Выбор оптимальных условий
градуирования методик рентгенофлуоресцентного анализа (РФА) фильтров,
нагруженных атмосферными аэрозолями
16.
Сердюк
О. С. Проблема ПАУ и их содержание в природных средах Кузбасса
